

�l���r�g��2019-12-28���ٷ���t�WՓ���g�[��1��
ժ Ҫ�� ժҪ �����Ը�ð�������Q���в���, ���������ݡ��i(Sus)�ȶ�N�����Լ��˵ĸ�Ⱦ�Ͱl��, ����Ҫ����������ԭ. �����, ��N���������в����ij��F���������緶���ȵ�����, �����˸�Ⱦ�����в�������, �ӄ��������в����Ĺ����l���WΣ��. ���в�����Ⱦ����
����ժҪ �����Ը�ð�������Q���в���, ���������ݡ��i(Sus)�ȶ�N�����Լ��˵ĸ�Ⱦ�Ͱl��, ����Ҫ����������ԭ. �����, ��N���������в����ij��F���������緶���ȵ�����, �����˸�Ⱦ�����в�������, �ӄ��������в����Ĺ����l���WΣ��. ���в�����Ⱦ������, ����Ҫ��������ϵ�y������, Ҳ���Ԍ����И���ϵ�y�����P���Y, �c�������A���������P. ���ľC���������в����������в��������Ե����P�о��Mչ, �����в������P���X�����R�����c�����в��������И���ϵ�y��;��, �Լ��l�������Եķ��әC�ƵȎׂ�������U�����в������l�����Ե��^���c�C��, ���ڼ���˺������в��������Ե��J�R������.
�����P�I�~ �����, ������, ��, ��
���������Ը�ð����(influenza virus)���Q���в���, ������𤲡����(Orthomyxoviridae), ��һ�N����Ĥ���ֹ��εĆι�ؓ�RNA����. �����˵���(nuclear protein, NP)�����|����(matrix protein, M)��ԭ�ԵIJ, �Ɍ����в����֞�A, B, C��D�Ĵ����. A�����в����������������P������N������ЏV������, �����N����; B�����в����H�����������; C�����в�����Ҫ���˼��iȺ������; ���°l�F��D�����в�����Ҫ��Ⱦ�i��ţ[1,2]. ����A�����в������ͱ���, ����Ѫ���غ�����ø�IJ�ͬ, ���Ԍ���֞� H1~H18��N1~N11, ����H17N10��H18N11�քe�� 2009��2010����ʳ�������w�Ȱl�F[3,4]. ԓ�Ͳ����Ŀ�ԭ�����װl��׃��, ��������������Դ�����. Ŀǰ, ����vʷ�Ͽ���ۙ������5�����в���������, �քe��1918�����������д����С�1957��H2N2�������д����С�1968��H3N2������д����С�1977�� H1N1���_˹���к�2009��H1N1���д�����[5]. ����, ���в���ÿ�겻���M��, �a���µĿ�ԭ�Զ���, ��ɳ��m�����в�������������. 2009��pH1N1���в�����H3N2�������в����Ǯ�ǰ��Ҫ���еļ��������в�������(http://www.who.int/en/news-room/fact-sheets/ detail/influenza-(seasonal)). ֵ��ע�����, ��1997���״Έ�������в���(avian influenza virus, AIV)��Ⱦ���¼��ԁ�, ԓ��������ͻ�ƷN�g���ϸ�Ⱦ���. ���� 2018��11��1��, �˸�ȾH5N1����AIV�����_�\860��, ����454������, �����ʞ�53%; H7N9���в�����2013�걬�l��, ����2018��11��7��, ������1567�˸�Ⱦ, ����615������, ���������ʳ��^39%(http://www.who. int/influenza/human_animal_interface). H9N2����AIV Ҳ���Ը�Ⱦ��, Ѫ��W�C�������ڱ��{�����Ⱥ�и�Ⱦ�ʿ����_��33.5%[6]. ���, A�����в���, �e�� H1N1, H3N2���������в�����H5, H7�Լ�H9���� AIV��������a���^�����{.
������������ָ���������И���ϵ�y��, ����ϵ�y����Ч����, ��������ϵ�y���P����������[7]. ���в�����Ⱦ������, ��Ҫ�������ϵ�y����, �ЕrҲ�����º���ϵ�y��ļ���, ���И���ϵ�y���P���Y[8,9], ���²������, �A����. H1N1��H3N2���������в������������׃����ЋD���X��, �����˻��ߵ�������[10,11]. ��Щ��, ��H5N1, H7N9�Լ�H9N2�ȁ��� AIV��Ⱦ�˵IJ����M���R�������{��l�F, ��Ⱦ����Ҳ�����F��ϵ�y���l�Y, ��Ҋ�X�ס��@�ʡ����ϾC����[12~14]. �����ڌ������в����������о��M�оC���Ļ��A��, �Mһ�������������в��������������P�о��Mչ, �C���U���˲�ͬ���в��������������P�X���İl�����c���l���lչ�ķ��әC��, ���ڞ����в������P�X���ķ����ṩ�����Y��.
����1 A�����в����������Լ���������X��
����1.1 �����в����������Լ���������X��
���������в�����Ⱦ�����˵ļ����X��, �ַQ�������P���X��(influenza associated encephalitis/encephalopathy, IAE), ��ָ�ڼ������в�����Ⱦ�^���а��S�И���ϵ�y(central nervous system, CNS)�����ϵK��һ�N�R���C����, �䌧�µIJ����p�ز�һ, ���͵��R���Y��鼱�Ըߟ��ͻ�l�@��, ���ߕ������M���������������. ���н�1/4�IJ����l�����Q���p�����X����, �Q֮�鼱�ԉ������X��(acute necrotizing encephalopathy, ANE)[15,16]. ����1918�����������д����Еr��, �Ͱl�F��˯���X���c�������P. 1957�ꁆ�����д����к���ʽ�����IAE[17]. ���߳��l�Y���ߟ�, ֮���ژO�̵ĕr�g�ȳ��F�d�������R�ϵK����ϵ�y�C����, �A��O�䲻��. ���в�����Ⱦ�C�w��, �����²�ͬ�̶ȵ�����p�����߇��ص��X��. ���в���������X�����ЋD�͋��׃�����鳣Ҋ, ���ؕr������������. 1996~2000��, ���в�������Ĵ��X�����ձ��V������, ÿ����100~500����Ⱦ���в����Ļ��߱��F�����X�İY��[18]. �ֻ������g��5�q����, ��Ҫ�R���Y����F��d�B�����R��ʧ�ͻ��Ե�, �����ʼs�� 30%[19].
���������ձ�, ���в������������Һ͵^�����^����Ҳ��������X��CNS�C����. 2009��pH1N1���в������l���g, �кܶ�CNS�����Ɂy�IJ������, �����˹������Pע[20~23]. ���߳����F���p�����R��ʧ�������e�y����F���X���R���Y��. ����ǰ, ��������Ը���������������. ��������, CNS�C�������»��ߵ��Ԛ������@���. �@Щ���߶������ˊW˾���f�M���ί�, �@һˎ���ʹ��Ҳ�п�����ʹ�����e�y[24]. ��ԭ�W�{���о��l�F, ���в����������И���ϵ�y�p���Y��ߵ��X��Һ�����X�б��z�y��, ���а���H1N1��H3N2�������в���[11,25,26]. ����֮��, ���в���������ϵ�y�����������ɭ�C�����Ͱd�B�ȇ��صĺ��z�Y[27,28].
�������в�������İl��Ҳ�����������Xˮ�[, �������X��. �@����ڋ��׃����^���l��, ���͵��R���Y����F�鼱�Ըߟ��ͻ�l�@�ʡ����R��ʧ���d�B���B�ȉ����ߵ�[29]. �����X�������»����L�r�g�����R��ʧ, ���ߵĻ���ָ��С�ڵ���13, ���m�r�g�L�� 24 h.
���������X���İl����Ҫ�c���в����錧���^���������ӵı��_���P[29]. ���C�w�����в������w�|�r(�美�a������Ĥ���ס�RAN�Y�ϵ���2�������wø����A�ؙ�ͪ�D��ø�Ļ���l��ͻ׃), ���в�����Ⱦ�C�w��t�����������ԉ������X��[30~32]. �����������ӵķ���(TNF-α��IL-6)�����´��X�������M��Ѫ�܃�Ƥ�p�������|�����{��, �M���Ɖ�Ѫ�X����, �����Xˮ�[��ȫ�������ٓp��[27]. Ѫ-�X���ϵ��Ɖĕ��������Լ����������ʹ��������|�M���X��Һ; �����w����ˎ (�p�ȷ����c�ͼל���)��ʹ��Ҳ�������X�����ߵ�������[29]. ���������^��Ҋ���X��֮��, ���в�����Ⱦ�C�w߀�����������X���C����, ���������X�����S�p�Ȱd�B���t�l�ԔUɢ(acute encephalopathy with biphasic seizures and late reduced diffusion, AESD)�Լ��R���p�X�����S����ĊA���p��(clinically mild encephalitis/encephalopathy with a reversible splenial lesion, MERS)��, ͬ��ֵ���Pע[33,34].
����1.2 �����в����������Լ���������X��
��������ڸ�Ⱦ���²���H5N1����AIV��, �����F�����@���Y��[35,36]. �о��l�F, ���²���H5N1���� AIV��Ⱦ�u��, ��Ѫ�܃�Ƥ�����к����H����, ����ѪҺ��������ͬ�M���Č��|����, �������X������[37]. �u������Ⱦ���²���H5N1����AIV������F���И���ϵ�y�Ɂy��ȫ�����ӡ����wʧȥƽ����^�i����R���Y��[38,39], ���Ӹ�Ⱦ���²���H5N1���� AIV������F�^�i��б���������������ԵȰY��[40]. �M��Ŀǰ߀�]�����ȾH7N9���в������F�Y������P���, �������о�����, �ĸ�ȾH7N9���ݵĴ��X�п��ԙz�y���^�ߵζȵ����в���[41], �������Пo�Y��ij��F, �����Mһ���{��.
���������, �S�������в�������ذl����������, �����ѽ���Խ�˷N�g�ϵK, �@���˸�Ⱦ������������. H9N2, H5Nx��H7N9����AIV��Ⱦ�˵IJ������^�����[14,42~44]. �����@�N����AIV��, H10N7����AIVҲ�����ڲ�������w�Ȳ����m��֮��, �ʬF�V���ĽM������, ����ͻ��Ѫ�X���ϸ�Ⱦ���������ϵ�y[45]. ���˸�ȾH5N1�����²��������е��R�����������@ʾ, ��236���˸�Ⱦ�����в�����, 74�����F���� (31.36%), 59�����F���R�ϵK(25%)���Y��[12]. ��ԭ�W�����C��, ��1997����۰l���˸�Ⱦ���������g, �ĵ������˸�Ⱦ�����гɹ����x����H5N1����AIV, ԓ���x����Ќ�С��(Mus musculus)������[46]. ����, Pringproa����[47]�����w���Ⱦ����о��@ʾ, �˵���Ԫ������H5N1�����²��������в����dz�����, ���Ҳ�����Ⱦ����@�����{TNF-α��ˮƽ, Ӱ���������ֳ�ͷֻ�. ��Ҋ, �����в����X�����Dz������И���ϵ�y��ֱ�����u, ͬ�rҲ�Ǽ������ӽ錧�ķ���. ����, ����Ⱦ��ԴH7N9������6���������R�������@ʾ, ����2���ʬF��ϵ�y���l�Y[13]. �w���о�����, �c2009��pH1N1�������, H7N9�������в�������Ⱦ�����z�|��������Ԫ, ������������Ч�D䛺͏���[44].
�����M�������в�����Ⱦ�ˌ��µĸ������������ˏV���Pע, ����ԓ����������Y��s��������ҕ. �@�N�������ʿ����c�����в������������������P. ���, �҂���ԓ�������в����������Խo��߶���ҕ, ������̽ӑ�����в����������в��������Եī@���Լ������И��²��C�ƵĮ�ͬ, ��̽����ͬ�ķ��δ�ʩ.
����2 ���в��������И���ϵ�y��;��
�����c���������Բ���һ��, ���������Ե����в���Ҳ��ͨ�^��N;�����֙C�w���И���ϵ�y. �����в��������И���ϵ�y;�����о������������ⲡ���������ԙC���Լ��_�l��Ч���������ֹ���в������C�w�И���ϵ�y�ĸ�Ⱦ. �И���ϵ�y����Ѫ�X���ϱ��o�ęC�w�خ�������, ���, ������Ҫ��ԽѪ�X���������И���ϵ�y. Ŀǰ�J��, ���в�����ͨ�^�����ͼ����g϶�ɷN��ʽ��ԽѪ�X����, ǰ�ߞ�ֱ�Ӹ�ȾѪ�X���ϽM�ɼ����Ϳ缚��;��, ���ߞ��Ɖă�Ƥ�����g�o���B�Ӽ�“������ľ�R”;��. ���˴�ԽѪ�X������, ���в���߀����ͨ�^��;��ֱ�����֙C�w���И���ϵ�y(�D1).
����2.1 ���в�����ԽѪ�X���ϵăɷN;��
����Ѫ�X����λ��Ѫ�ܺ��X�M��֮�g, �����x���Ե���ֹһЩ���|��ѪҺ�M����X, ��Ѫ-�X��Ѫ-�X��Һ���X��Һ-�X���N���ϵĿ��Q. ����@�R���^��Ѫ�X���ϵij��Y���l�F: Ѫ�X������Ҫ���XѪ�܃�Ƥ����(brain microvascular endothelial cell, BMEC)���会���g�ľo���B�ӡ���Ĥ��С�z�|�������ܼ����������z�|�������ɵ����z�|Ĥ����[48,49]. ����BMEC ��Ѫ�X���ϵ���Ҫ�Y��, ��ͨ�^픶����cѪ�����|, ͨ�^�������c�X����ͨ, BMEC֮�g�ľo���B�ӿ���Ч���Ƽ�����·;�������|�D�\[50]. ����֮��, С�z�|�������ڲ�ԭ�w�̼���ጷż�������, �������ԭ�w; �ܼ������{��Ѫ�ܵ��γɼ�Ѫ�ܵ�������; �����z�|����ͨ�^���ڿ��������Ӂ����M�o���B�Ӽ�Ѫ�X���ϵ�������[50]. �@Щ�Y��������Ч���Ʋ��������И���ϵ�y.
����Ѫ�X���ϿɾS���И���ϵ�y���B, ����ѪҺ�д������ԭ�w������; Ȼ�����ֲ����ɴ�ԽѪ�X���������И���ϵ�y, �����И������Ɂy�����Է���. ���в�����ԽѪ�X���Ϻ�ͨ�^���浰���c�X�������浰�������, �錧���������ӵı��_�����M��������Ԫ�е���Ч����, ��K������Ԫ׃�ԉ���, �����@�ʡ����R�ϵK���X�װY��. ���в�����Ҫͨ�^����;���ͼ����g϶;����ԽѪ�X����.
����(1) ����;��. BMEC��Ѫ�X���ϵ���Ҫ�Y��, �� BMEC����Ч��Ⱦ�Dz��������И���ϵ�y�ؽ�֮·֮һ[51]; �˶�������JC[52]������T��������1��[53]���ɸ�Ⱦ���XѪ�܃�Ƥ����(human brain microvascular endothelial cell, HBMEC), ����HBMEC�ȏ��Ʋ�ጷ��Ӵ�����, �����Ԫ׃���c����, Ȼ�����в����Ƿ�Ҳ��ͨ�^��ȾHBMEC�����������И���ϵ�y��δҊ���. ����, ����о��������в������Ը�ȾС�z�|�������ܼ����������z�|����, �@Щ����Ҳ��Ѫ�X���ϵĽM�ɲ���[44,47]. ���, ���в�������ͨ�^��Ⱦ�@Щ������ԽѪ�X����.
��������, ������r��Ѫ�X�����ǷǝB�Ե�, �����ڶ�N����Ŀ缚���D�\����, ������c��������[50]. Verma����[54]�����w��Ѫ�X����ģ��, �l�F�����_����������BMEC�ľް������, �ڲ��Ɖ�Ѫ�X���������Ե�ǰ���¿ɴ�ԽѪ�X����. BMEC�ľް����������ԓ�����Ļ������, ���Sһ���̶���Ҳ�����в�����ԽѪ�X���ϡ������И���ϵ�y�ṩ����Ч��;��.
����(2) �����g϶;��. BMEC�g�ľo���B���ǾS��Ѫ�X���ϽY���c���������ԵĻ��A, ���{�����|�\ݔ�����Ʋ�ԭ�wͨ�^������·;���M���И���ϵ�y. �o���B�����B��𤸽���ӡ����]�����]�ϵ��ȶ�N��Ĥ���M��, ͨ�^�o���B�ӷ��ӵȹ̶������ڃ�Ƥ������[49]. ���в����ĸ�Ⱦ���Ɖľo���B��, ���¾o���B�ӵ�ͨ�ԉ���, ʹ�����ɴ�ԽѪ�X�������ֲ���Ⱦ�И���ϵ�y.
����Ѫ�X����̎�������ӵı��_�c��Ч��֮�g��ƽ�����e�C���s��. ͨ����r��, ���в����e��H5N1�� H7N9����AIV��Ⱦ�����z�|�����ɴ̼��������ӵ�ጷ�, ��IL-1β, IL-6, IFN-λ��TNFα[44,47]. �����������ӵĮa�������¾o���B���g��ͨ������, һ���̶����Ɖ���Ѫ�X���ϵ�������, ���M���в������И���ϵ�y�����ֺ�Ⱦ. BMEC���ܼ����������z�|�����������Ⱦ��ɮa��������������. ��ͬ�������ӵ����ÙC�Ƹ�����ͬ, ��Ѫ�X���ϵ�Ӱ�Ҳ��ͬ. �����_������Ⱦ�����z�|�����r�ɮa�����|���ٵ���ø (matrix metalloproteinase, MMP), MMP��ͨ�^ֱ�ӽ���o���B��, ���Ɖ�Ѫ�X����, ���ٲ������И���ϵ�y�ĸ�Ⱦ[55]; ��IFN-β�t�ɷ����o���B��, ������ BMEC�е�TAM(Tyro3, Ax1��Mertk)���w��fͬ�ɔ_�ص�����, �����o���B�ӵķ�����, �Ķ��S��Ѫ�X���ϵ�������[55].
��������, ����߀��ͨ�^“������ľ�R”;�������И���ϵ�y, ����Ⱦ������, �ɰ����y����ԽѪ�X����. ����ȱ�ݲ���(����������ȱ�ݲ������������ȱ�ݲ����Ϳ������@һ;��, �ɱ���Ⱦ�Ćκ˼�������ɼ����y����ԽѪ�X����[55]. ���о�����, H5N1����AIV�������Ø�ͻ�������“�\�d����”��Ⱦ�����K��, �����X, ���п��ܾ�������“������ľ�R”;�������И���ϵ�y[56].
����2.2 ��;��
��������ͨ�^����;���ͼ����g϶;����ԽѪ�X���������И���ϵ�y��, ���в���߀��ͨ�^��ͨ·ֱ�����ֲ��������И���ϵ�y. ��С���w�ȵ��о��Y������, ���в����ȿ�ͨ�^��ǻ����������������С����И���ϵ�y[44,57,58], Ҳ��ͨ�^�β��������ͽ���������С����И���ϵ�y[46]. ��ѩ����, ���²���H5N1����AIV�܉��Ⱦ���ı��Ĥ���w��Ԫ(olfactory receptor neurons, ORNs), ORNs����һ��ͨ�^�Y������쵽����ͻ�|��ӵ��Sͻ, ���@�����������, ��Ⱦ�����е��Sͻͻ�|������, �M���������И���ϵ�y[59]. Ŀǰ�����о��������²��������в��������Sͻ�g�M�Ђ���[60,61], �� ORNs�ĸ�Ⱦ��H5N1����AIV�����И���ϵ�y�ṩ�˸�ֱ�ӵ�·��[62]. �����w��, ���в���Ҳ��������ͨ·����ݏ����֙C�w�И���ϵ�y. �R����, ����һ�����߹��ܲ�ȫ�ă�ͯ�w�Ȱl�F������H3N2�������в�����ͨ�^����ͨ·�����И���ϵ�y[63]. Simon����[64]����^һ������, �l�F���������ڸ�Ⱦ���в�����, ��δ���F�κκ���ϵ�y�������P�Y��, �����F���������X�İY��, �������ęz�y�Y���l�F, �����ڲ��˵ı�ϴҺ���X�M���Йz�y������, ���ڷβ����X��Һ�о�δ�z�y�������Ĵ���. ����֮��, �R����߀�Ѓ����и��²���H5N1����AIV�������И���ϵ�y���Dz��]���������غ����������IJ������(2 ����ͯ�Ї��ص��XĤ���Ǜ]�к���ϵ�y����), �C�����в�����ͨ�^��ͨ·�������И���ϵ�y[65].
�����ɴ˿�Ҋ, ���в�������ͨ�^��N;�������������И���ϵ�y. Ȼ��, �����в����������в����Ƿ���ه��ͬ�ĸ�Ⱦ;����δ��֪, Ŀǰ�о����������в���ƫ��������;�������������И���ϵ�y, ����w��ԭ���д�̽��. ����, ��Щ�������в����M�����Ե�������������������F����Ѫ�Y, �@���S�����������в����������И���ϵ�y�����{. ���, �����O����ɲ���Ѫ�Y�������в����o����ҕ.
����3 Ӱ����в��������Ե��P�I����
����3.1 �����P�I����Ƭ�μ�����λ�c
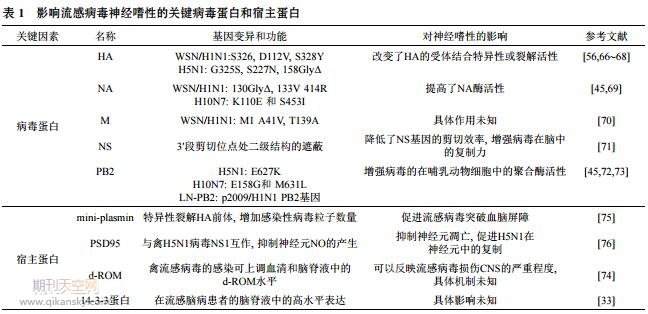
����С�����鲸�����ģ��, �о����в�������ϵ�y������;����Ӱ������Եķ��әC�Ƶ�. �c���в�����Ⱦ����ϵ�y�ķ��әC���о����, ���в��������ԙC���о���������. ���������Ĉ��, ���l�F���в�����Ѫ���ػ���(HA)������ø����(NA)�����|������(M)�Լ��ǽY������(NS)Ƭ�������������аl�]����Ҫ������. �����@�ׂ�Ƭ����, �ۺ�øPB2�����侎�a���������в����������Կ������P�I����(��1).
����(1) HA������. ���в�����HA����, ���a�����ı��浰��Ѫ����. HA���錧���в���������������Һ�����w������, �����в�����Ⱦ���������ĵ�һ��. �ڲ��������^����, HA��mRNA�����g��HA0, HA0 ��ˮ���HA1��HA2���^���Е�����λ��HA2-Nĩ�˵�“�ں���(fusion peptide)”�Įa��. ������r��, �ں��ijʭh��[77], ��HA̎�����ԗl���r, ��h��Y���D���������Y��, �����ںϵ�����������������wĤ��, ���Ĥ�ں��^��[78]. HA�����ѽ���ԛQ�������в����ĸ�Ⱦ��[79]. Nakajima����[80]���w����Ԫ�������C����HA���ѽ⌦���в��������Եī@�þ�����Ҫ����, �о��l�F���в�����HA�ڲ�ͬ�ļ�������о��в�ͬ���ѽ����, HA�ĸ��ѽ����ʹ�ò����܉��ڲ�����������Ч����, �������Ӵ��������ӵĽM�b. Zhang����[66]�����H5N1 HA�ѽ�λ�c̎325λ (P6λ)�z���������˲���HA���ѽ����, ʹ�����в����@���ˌ�С�������. HA���A�������ѽ�λ�c�Ĵ���Ҳؕ�I�����в�����ѩ����������[67]. �� WSN/H1N1������, ����HA�ѽ�λ�cP2λ���Ұ��� (328Y)��Q��H1�����ϳ�Ҋ�Ľz�����, ������С���X�еď��������@������, �f��328Y��WSN/H1N1���������������P��Ҫ[68]. ֵ��ע�����, ���˞���ڼ�����H3N2������������A�������ѽ�λ�c, �������f�o���@���ڲ�������w�ȵ�������, �C�����A�������ѽ�λ�c�������в������������DZ�Ҫ����֗l��[67]. ���, HA���w�Y��λ�cҲ�����в�����������ʮ����Ҫ. Yen����[56]�l�FA/Vietnam/ 1203/04(H5N1)����HA-S227N��158λȥ�ǻ�����, �������X�еď��Ƶζ����@�½�, ��Ⱦ������С����Y����ʧ, ���������w�Y�υ^�����@һ�^���е���Ҫ����.
����(2) NA������. ����ø����(NA)���a��������һ�����浰��, ����ø�����ǻ���������ø, �ܴ���Һ��ĩ�˚�������������ϵĚ���֮�gͪ���I���ѽ�, ���M�Ӵ��������ӵij�ѿ[81]. ����ø���J���ǛQ��WSN/H1N1���������Ե���һ�P�I����Ƭ��, NA-Cĩ�˾��нY���w�ܵ���øԭ������, 146 λ�ǻ���λ�c��ȱʧ������NA�Y���w�ܵ���øԭ������, �����w�ܵ���øԭ�D�����w�ܵ���ø, ���MHA ���ѽ�, �Ķ�ʹ������С���������[69]. ���������Ե�H10N7���m���Զ����NA����Ҳ���F�ɂ��P�I�İ�����׃��, K110E��S453I. ����K110E��ͻ׃�@�������˲���������ø����, �mȻ�Ϊ��� K110Eͻ׃��������������������������, �������cPB2�ϵ�λ�c�fͬͻ׃�r, ���Ԍ��²�����С���И���ϵ�y�ĸ�Ⱦ[45]. ����, Maurizi[82]�J�� 1918�����д���������ĸ���������Ҫ�����ڲ������˵�����, ���в�������ø�ķN����в������������P�I����, Ȼ��ԓ�о����]�нo�����w�Č���C��. ����ø�����в��������Եī@�þ����������, ����Ҫ�Mһ��̽��.
����(3) M��NS������. ���в�����M��NS������ɾ��a�ɷN��������, �քe��M1, M2, NS1��NS2. M1���Ľ��x���M�˲���vRNP�����; M1���כQ�������в����ď�������[83]. NS1��NS2�����������в����ăɂ��ǽY������, �����в��������������������^���аl�]��Ҫ����[84], ����, NS2����Ҳ�܉��cM1����ֱ�ӻ���, ���c�Ӵ��������ӵĽM�b�^��[85]. M�� NS�����ƺ�Ҳһ���̶��ϛQ�������в�����������. ���о����, M141λ���i�����139λ�ı����ጦ WSN/H1N1���������Եī@����Q������, ��������w���ÙC���Բ����[70]. ����, ���в��������^����, �ǽY������NS1��NS2����������ҲӰ��������ď��ƺ��D�ˮƽ, ����Ҳ�Q���˲�����������. �о�����, �����������Ե�A/WS/33(H1N1)������ NS1�ı��_����NS2�ı��_ˮƽ; �෴, ���������Ե�WSN/H1N1����NS1�ı��_���@������NS2[71], ��ʾNS1���ĸ߱��_���S�����в��������Եī@��������Ҫ����.
����(4) �������������. ����֮��, �S���о�����, ���в����������Ȳ�����Ҳ���������Եī@�þ�����Ҫ����. �����������в���PB2 E627K׃����ͨ�^��߲����ڲ�����:���еľۺ�ø����, Ӱ�H5N1 �����в�����������������[72]. ����, Lin����[73]����Q����2009 pH1N1 PB2�����H5N1���� AIV�@���ˌ�С�������, ��Ҋ, ���в�������Ƭ��֮�g�IJ�������Ҳ�����в����@�������Ե���Ҫԭ��. ����, Zhang����[45]�����H10N7���m���Զ����PB2 E158G��M631LҲ��Ӱ�H10N7���������в�����������.
�����ɴ˿�Ҋ, ���в���HA, NA, PB2, M��NS�����������Ծ�����Ҫؕ�I. ���@Щ������, �����������в����������в�����ؕ�I������ͬ. ����о�����, �c����Ƭ�����, �ۺ�ø�����������в��������Եī@�����ƺ���������Ҫ������. ��Ҋ, ����������ԙC���о��������ڸ�ȫ���J�R���в������������в��������Ե�Ӱ�.
�������PՓ�����]��A�����в�������M1������
����ժҪ��A�����в�����һ�N���ЏV���������ʺܸߵIJ�������������ﶼ����˘O���Ӱ푡�M1��������S��A�����в��������ΑB�ĵ��ף���������������������Ҫ���ã�������w�Y���������д�̽ӑ����A�����в����Ļ�����������W�����M���˾C������������|����M1������W���ԡ����ܺͽY�������U����
SCISSCIAHCI